چرا دیابتیها به کرونای شدید مبتلا میشوند؟
آنان با یک مدل موش مبتلا به عفونت کروناویروس شروع کردند و دریافتند که آنزیم SETDB۲ در سلولهای ایمنی دخیل در واکنش التهابی موشهای آلوده به دیابت که ماکروفاژ نامیده میشود، کاهش یافته است. آنان بعدها همین مورد را در ماکروفاژهای تک سلولی در افراد مبتلا به دیابت و کووید-۱۹ شدید مشاهده کردند.
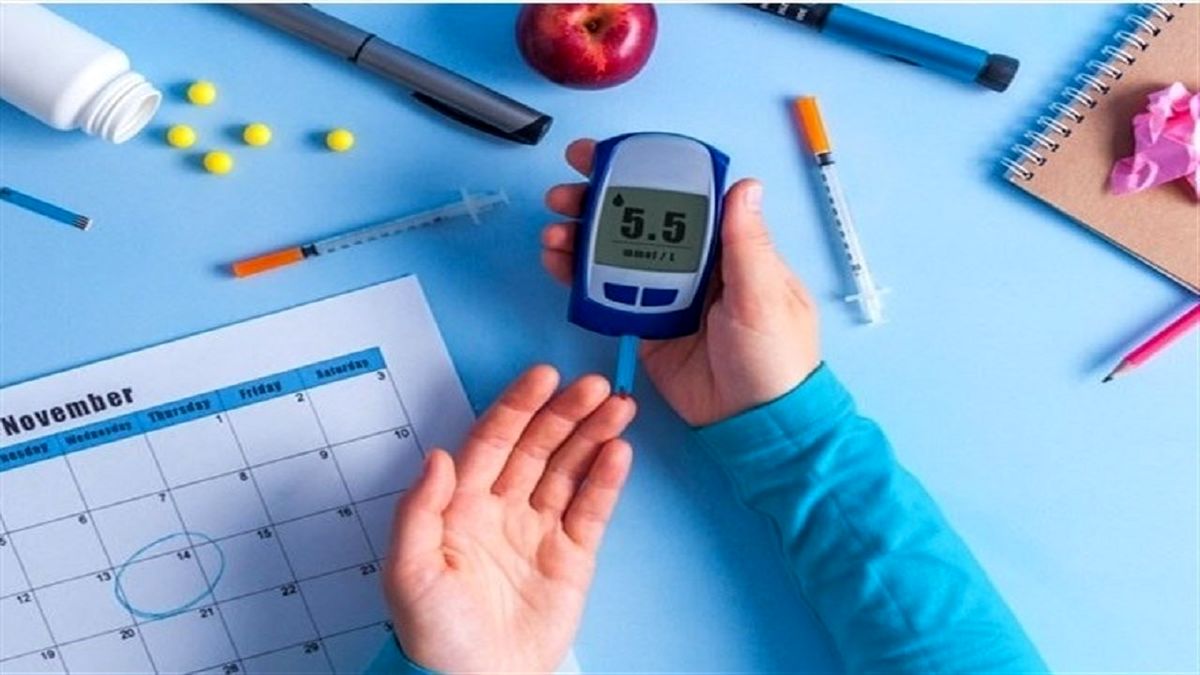
به گزارش منیبان؛ در طول همهگیری کووید-۱۹، پزشکان خاطرنشان کردند که برخی از بیماران در معرض خطر بیشتر ابتلا به بیماری شدید یا مرگ بر اثر عفونت کروناویروس قرار دارند. دیابت نوع ۲، بیماری است که بیش از ۱۰ درصد از جمعیت ایالاتمتحده را تحت تاثیر قرار میدهد و یکی از عوامل خطر اصلی برای بیماری شدید کووید-۱۹ است. نتایج تحقیقات جدید دانشگاه میشیگان آمریکا، دلیل این امر را کشف کرد و درمان بالقوه در این زمینه ارائه خواهد کرد.
بهنظر میرسد علت آنزیمی به نام SETDB۲ باشد. همین آنزیم در زخمهای بهبود نیافته و التهابی موجود در افراد مبتلا به دیابت نقش دارد. محقق، کاترین گالاگر، پزشک بخشهای جراحی و میکروبیولوژی و ایمونولوژی میشیگان و دکتر جیمز ملوین و همکاران وی تصمیم گرفتند که ارتباط احتمالی بین آنزیم و التهاب کنترلنشده را که از نزدیک در بیماران مبتلا به کووید در آیسییو (بخش مراقبتهای ویژه) مشاهده کردهاند را بررسی کنند.
آنان با یک مدل موش مبتلا به عفونت کروناویروس شروع کردند و دریافتند که آنزیم SETDB۲ در سلولهای ایمنی دخیل در واکنش التهابی موشهای آلوده به دیابت که ماکروفاژ نامیده میشود، کاهش یافته است. آنان بعدها همین مورد را در ماکروفاژهای تک سلولی در افراد مبتلا به دیابت و کووید-۱۹ شدید مشاهده کردند.ملوین میگوید: «ما فکر میکنیم دلیلی دارد که این بیماران دچار طوفان سیتوکین (آزادسازی بیش از حد مولکول پروتئینی سیتوکین) میشوند.»
ملوین و گالاگر اظهار کردند: در مدلهای موش و انسان، با کاهش آنزیم SETDB۲، التهاب افزایش یافت. علاوه بر این، آنان فاش کردند، مسیری به نام JAK۱/STAT۳ این آنزیم را در ماکروفاژها در طول عفونت کرونا تنظیم میکند. (واسطه سیتوکینها، جانوس کینازها (Janus kinases, JAKs) هستند، این کینازها، پس از فعال شدن باعث فسفریله شدن پروتئین STAT میشوند که در تکامل و عملکرد دستگاه ایمنی، تحمل ایمنی و بقای تومور نقش دارند.)
روی هم رفته، نتایج به یک مسیر درمانی بالقوه اشاره میکند. یافتههای قبلی آزمایشگاه نشان داد که اینترفرون، یک سیتوکین مهم برای ایمنی ویروسی، آنزیم SETDB۲ را در پاسخ به ترمیم زخم افزایش میدهد. آنان در تحقیق جدید خود دریافتند که سرم خون بیماران در بخش آیسییو مبتلا به دیابت و کووید-۱۹ شدید، سطح اینترفرون بتا را در مقایسه با بیماران بدون دیابت کاهش داده است. (اینترفرون، پروتئینی که توسط سلولهای حیوانی آزاد میشود بهطور معمول در پاسخ به ورود ویروس است و خاصیت جلوگیری از تکثیر ویروس را دارد.)
گالاگر گفت: «اینترفرون در طول همهگیری بهعنوان یک درمان بالقوه مورد مطالعه قرار گرفته و تلاشها برای افزایش یا کاهش سطح اینترفرون صورت گرفته است. احساس من این است که اثربخشی آن بهعنوان یک درمان هم برای بیمار و هم برای زمانبندی، خاص خواهد بود.»
گروه تحقیقاتی برای آزمایش این مورد، اینترفرون بتا را برای موشهای دیابتی آلوده به کروناویروس تجویز کردند و مشاهده کردند که آنها قادر به افزایش SETDB۲ و کاهش سیتوکینهای التهابی هستند.گالاگر توضیح داد: ما در حال کار روی آنچه آنزیم SETDB۲ کنترل میکند، هستیم. این آنزیم به نوعی تنظیمکننده اصلی بسیاری از این سیتوکینهای التهابی مانند IL-۱B، TNF alpha و IL- ۶ است که شنیده میشود طی کووید-۱۹ در حال افزایش هستند.
با نگاه از بالا به آنچه که SETDB۲ را کنترل میکند، میتوان دریافت که اینترفرون در انتهای بالای این جریان قرار دارد و جانوس کیناز ۱ و پروتئین STAT۳ در وسط قرار دارند. اینترفرون هر دو را افزایش میدهد و موجب افزایش آنزیم SETDB۲ بگونهای آبشاری میشود.وی افزود: این مهم است زیرا شناسایی این مسیر، راههای بالقوه دیگری را برای هدف قرار دادن آنزیم ارائه میدهد.
ملوین و گالاگر امیدوارند، یافتههای این تحقیق به آزمایشهای بالینی مداوم اینترفرون یا سایر اجزای پایین دست مسیر، ازجمله اهداف اپیژنتیک، برای کووید-۱۹ منجر شود. کار آنان همچنین نیاز به درک زمانبندی و درمان ویژه سلول را بیان و کاربرد آن را بر اساس شرایط زمینهای بیماران، بهویژه بیماران مبتلا به دیابت متناسب میکند.
ملوین گفت: «نتایج تحقیق ما نشان میدهد، شاید اگر بتوانیم بیماران مبتلا به دیابت را با اینترفرون، بهویژه در اوایل عفونت، هدف قرار دهیم بهراستی میتوانیم تفاوت بزرگی در درمان ایجاد کنیم.»